شركة أمريكية تسحب دواء التصلب الجانبي الضموري بعد فشل تجربته
ا ف ب - الأمة برس
2024-04-07
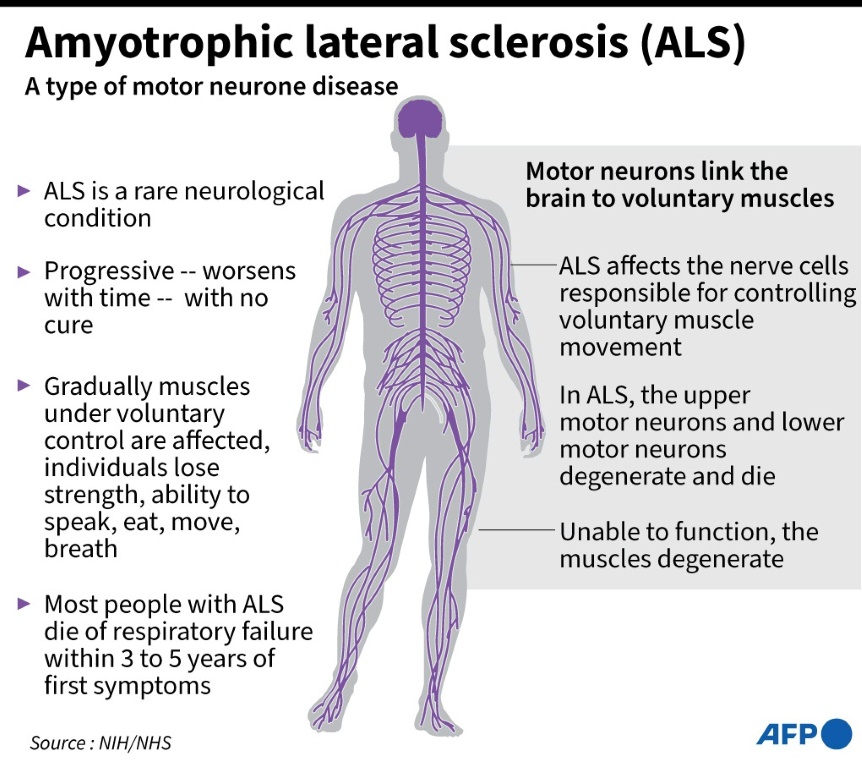
أعلنت شركة أميليكس للصناعات الدوائية أنها ستسحب علاجها المعتمد ضد مرض التنكس العصبي القاتل ALS بعد أن وجدت البيانات السريرية عدم وجود دليل على نجاح الدواء.
وقالت الشركة الأمريكية في بيان لها إنها ستوقف تراخيص السوق الخاصة بعقار Relyvrio/Albrioza، باستخدام الأسماء التجارية للدواء في الأسواق الأمريكية والكندية.
وقال الرؤساء التنفيذيون المشاركون للشركة: "على الرغم من أن هذه لحظة صعبة بالنسبة لمجتمع التصلب الجانبي الضموري، فقد وصلنا إلى هذا المسار للأمام بالشراكة مع أصحاب المصلحة الذين سيتأثرون وبما يتماشى مع التزامنا الثابت تجاه الأشخاص الذين يعيشون مع التصلب الجانبي الضموري وأمراض التنكس العصبي الأخرى". جوشوا كوهين وجاستن كلي في بيان.
وقالت الشركة أيضًا إنها ستخفض قوتها العاملة "بحوالي 70 بالمائة" حيث ركزت على دواء تجريبي آخر للاستخدام ضد التصلب الجانبي الضموري، وعلى إعادة استخدام ريليفريو لحالات أخرى. وأضافت أنها ستواصل إتاحة عقار "ريليفريو" للمرضى الذين يرغبون في الاستمرار في استخدام العلاج، من خلال "برنامج دوائي مجاني".
تأتي هذه الأخبار في أعقاب بيانات من تجربة سريرية أجريت على 664 مريضًا بمرض التصلب الجانبي الضموري تم الإعلان عنها في مارس، والتي لم تجد فروقًا كبيرة في النتائج بين أولئك الموجودين في مجموعة العلاج وأولئك الذين تلقوا علاجًا وهميًا.
لقد كان ذلك بمثابة ضربة كبيرة للمرضى الذين يعانون من مرض التصلب الجانبي الضموري، والذي يطلق عليه أحيانا مرض لو جيريج على اسم لاعب البيسبول الشهير، والذي يدمر الخلايا العصبية في الدماغ والحبل الشوكي.
يؤثر التصلب الجانبي الضموري (ALS) على شخصين تقريبًا لكل 100.000 كل عام، مما يتسبب في فقدان تدريجي للوظيفة الحركية والإدراكية. يموت معظم المرضى في غضون خمس سنوات من تشخيصهم.
وكانت موافقة إدارة الغذاء والدواء الأمريكية على عقار ريليفريو في عام 2022 مثيرة للجدل واستندت إلى نتائج تجربة واحدة شملت 137 مشاركًا فقط.
لاحظت إدارة الغذاء والدواء نفسها أن هناك "شكوكًا متبقية حول أدلة الفعالية" - ولكن "نظرًا لطبيعة المرض الخطيرة والمهددة للحياة والاحتياجات الكبيرة غير الملباة، فإن هذا المستوى من عدم اليقين مقبول في هذه الحالة والنظر في هذه النتائج في سياق المرونة التنظيمية مناسب."
موافقة مجموعات المرضى
شنت مجموعات المناصرة أيضًا حملة كبرى لإرسال التماس إلى إدارة الغذاء والدواء الأمريكية يتضمن عشرات الآلاف من التوقيعات التي تحث على الموافقة. وبمجرد توفرها، أعلنت أميليكس عن قائمة أسعار مذهلة تبلغ 158 ألف دولار سنويًا في الولايات المتحدة، مما أثار انتقادات.
وراقبت مجموعات المرضى في أوروبا بيأس التأخير البيروقراطي.
وعندما أعلنت هيئة مراقبة المخدرات التابعة للاتحاد الأوروبي في وقت لاحق أنها ترفض استخدام دواء ريليفريو، تم انتقاد القرار باعتباره "إهانة" من قبل المرضى الفرنسيين الغاضبين، الذين يقولون إنهم "ليس لديهم وقت للانتظار". وفي وقت لاحق رضخت فرنسا وقدمت موافقة مشروطة في نوفمبر/تشرين الثاني.
وقالت جمعية التصلب الجانبي الضموري ومقرها الولايات المتحدة، والتي مارست ضغوطا من أجل الموافقة على الدواء ومولت مشروعه: "إننا نشيد بـ أميليكس لسحب Relyvrio من السوق، مع ضمان أن الأشخاص الذين يعانون من مرض التصلب الجانبي الضموري يمكنهم الحصول على الدواء إذا كانوا يعتقدون أنه يساعدهم". بحث.
وأضافت: "يمكن إتاحة علاجات آمنة وربما فعالة بسرعة حتى تؤكد المزيد من الأبحاث فعاليتها".
في الوقت الحالي، لم يتبق سوى عدد قليل من العلاجات المتاحة.
ريلوزول، الذي وافقت عليه إدارة الغذاء والدواء الأمريكية في عام 1995، يطيل العمر حوالي ثلاثة أشهر. تم العثور على Edaravone، الذي وافقت عليه إدارة الغذاء والدواء الأمريكية في عام 2017، لإبطاء تطور المرض وتحسين البقاء على قيد الحياة.
وفي عام 2023، وافقت الهيئة التنظيمية على tofersen، وهو علاج جيني يستهدف حالات التصلب الجانبي الضموري التي تنتج عن طفرات في جين SOD1.